國產疫苗受質疑 高端發出聲明自清:加速執行三期臨床試驗
2021-05-31 18:21 聯合報 / 記者林海/台北即時報導
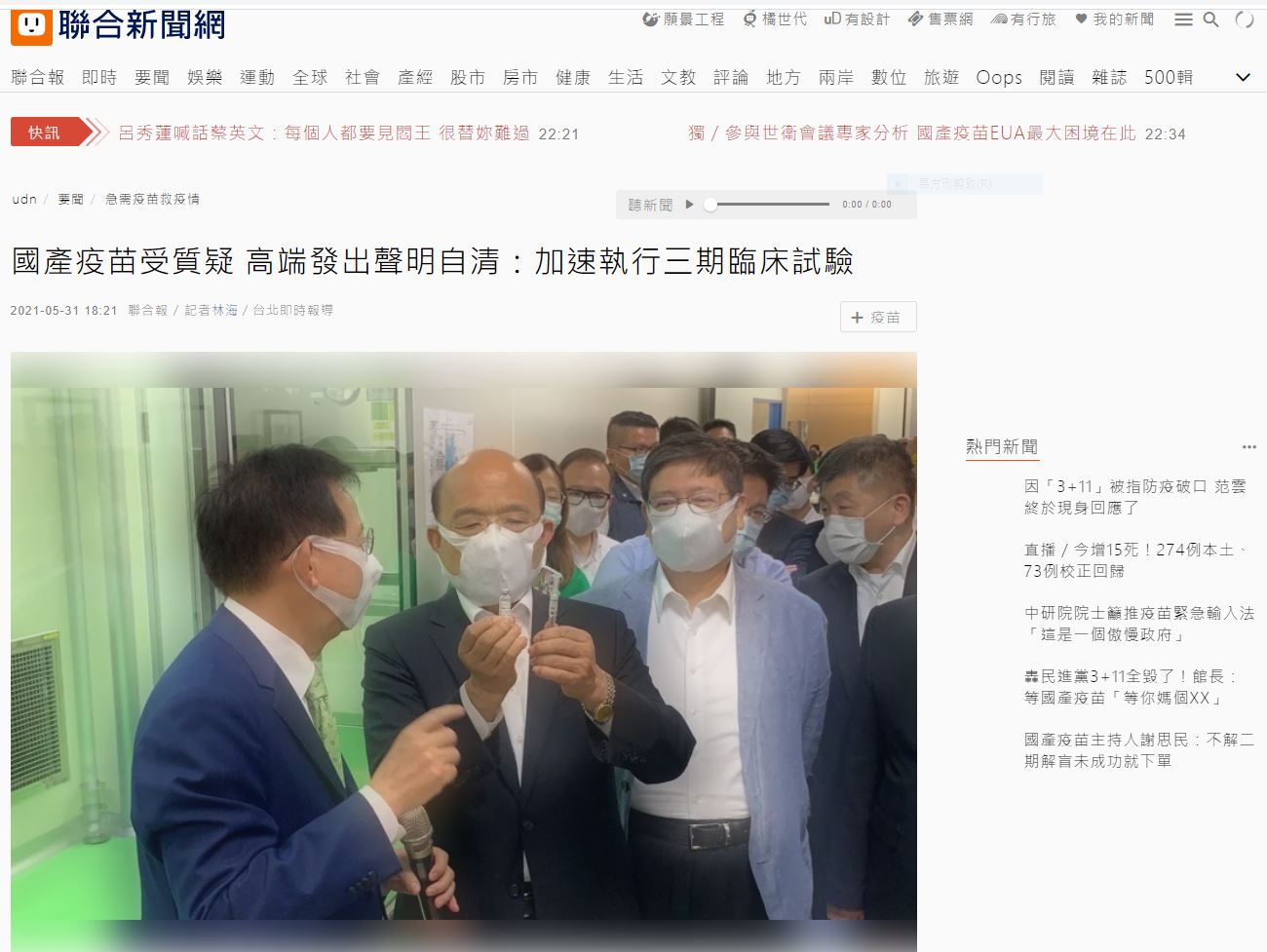
圖為行政院長蘇貞昌(左二)去年6月前往位於新竹生醫園區的高端疫苗公司視察。圖/聯合報系資料照
在二期臨床解盲之前,政府即與高端疫苗簽訂預購合約,將採購五百萬劑新冠肺炎疫苗,引發爭議。對此,高端今發出聲明表示,二期臨床實驗結果如符合預期,將加速執行符合國際規範的三期臨床試驗,以取得國際認證為目標。
高端聲明指出,國產疫苗為國內防疫布局中一環,為滿足國內防疫需求,期待台灣儘快取得不同國內外廠家的合法疫苗,以維護國民生命健康。
高端表示,二〇一六年起與美國國衛院(NIH)合作研發疫苗,去年初疫情爆發,就積極聯繫NIH並簽署授權合約,取得新冠肺炎候選疫苗及相關生物材料,於台灣進行研發及生產。
高端表示,執行中的二期臨床試驗依食藥署規範執行,解盲後結果將交由主管機關審查,而與疾管署簽訂的預採購合約,在安全性及有效性符合標準並取得核可後,才能交貨協助台灣防疫。
高端也說,二期臨床實驗結果如符合預期,將加速執行符合國際規範的三期臨床試驗,以取得國際認證為目標。