Charm_intg wrote:
冠狀病毒再怎麼變形狀(恕刪)
關於解藥部分,我看到兩篇新聞
關於清冠一號
清冠一號:世界熱銷,唯獨台灣買不到,關鍵在於模糊隱晦
簡單說中藥是針對症狀,國外並沒有說這可以解新冠,只說可以減緩症狀,但台灣媒體就高潮說可以對抗新冠。這概念就像假如我得愛滋免疫下降一直烙賽,我吃普拿疼不烙賽了,媒體就說普拿疼可以解愛滋這概念一樣
關於伊維菌素
抗寄生蟲藥「伊維菌素」將終結疫情?教授:奎寧的教訓還不夠嗎
你是否相信,就自己選擇吧,我非專業人士,分享一下我看完這整層樓一些文章去搜尋找到的~
lightphoto wrote:
你第一點還是我說的那樣,緊抓一個點來打不同時空背景的點,拿Alpha當初可防範的口號來打目前Delta的疫情,沒隨時間去檢討這理論基礎是否依然可靠說服我
請問我需要說服您什麼...?
我本篇的標題是 :「辯論」靠疫苗防疫是必輸的賽跑
請問你覺得靠疫苗一直打下去就會贏了嗎?
重申我的立場:
1) 不反對疫苗, 但對EUA實驗性疫苗風險持疑慮, 須謹慎使用疫苗策略
2) 疫苗打到20%高風險群即可, 不應推廣全民疫苗
3) 年輕人打疫苗根本得不償失, 長期後遺症後果不堪設想
4) 病毒會一直變種, 疫苗抵抗力不如天然免疫力和抗體
5) 回歸天然抗體與藥物治療才是根本長久之道
歡迎您針對我的立場來探討, 我隨時奉陪~
更多訊息: https://www.facebook.com/HankRS225
henrylai21 wrote:
這才是你所說的「真是不知所謂」吧?
還是,你根本不知道疫苗後遺症有哪些....? (資訊不對稱?)
你是真傻。?還是裝傻? 然後全世界那麼多專家,包含美國,中國,聯合國的專家都沒有你懂? 就你最懂?
誰不知道疫苗後遺症? 那你知道新冠如果 輕症,即使好了。其實也沒完全好,甚至很多男性會損失生殖能力這些後遺症嗎?
根據國外一年多追蹤研究,權威期刊「自然」統計,有三成確診者出現後遺症,包括呼吸困難、肺功能衰退、頭痛、腦力衰退等。
那你所推崇的支持療法,然後不要打新冠疫苗,在感染後,是否會有這些後遺症? 那到底是 隨時都會感染新冠,然後透過支持療法比較好,還是 直接打疫苗,避免感染,或感染後不會轉重症比較好?
其實早就有答案。 人家 自然雜誌,柳葉刀,然後包含世界主流醫學認知也是認為要打疫苗的。 然後這些人都不懂?就你懂? 你是懂王?
真是白癡。 我不會再回這樓文了......跟這種白癡 沒什麼好討論。
lightphoto wrote:
關於伊維菌素
抗寄生蟲藥「伊維菌素」將終結疫情?教授:奎寧的教訓還不夠嗎
這位教授的文我看過, 他這種論述法其實與「事實查核中心」的手法差異不大
用雞蛋裡挑骨頭的方式找對手的部分瑕疵,藉以否定整段論述
他只有提出對對方不利的部分出來攻擊,但他卻也無視大規模實驗數據的結果(這個部分他推給「需要再做進一步研究」敷衍過去)
我只能說,目前的主流權威對於新冠解藥實驗是用放大鏡去找瑕疵,對疫苗副作用傷害是選擇性視而不見,這對比態度差距非常明顯,你如果看不出來這個趨勢,選擇相信幾個新聞,那也無妨,時間會慢慢證明一切的
很多科學權威並不如你所想得那樣善良而單純
參考:「新冠無藥可醫」是整個COVID-19疫情最大的騙局!
Ivermectin全球民間醫學報告彙總: (點我查看)
更多訊息: https://www.facebook.com/HankRS225
henrylai21 wrote:
參考必讀:
1) 疫苗無法對抗變種
2) 天然免疫力比疫苗更重要
3) 天然抗體比疫苗強13倍!
4) 疫苗如何導致死亡傷殘?
5) Covid無藥可醫其實是謊言
6) 台灣人DNA優勢可以提早結束疫情
7) 哪些人打疫苗容易猝死?
1. 原因是 這個病毒的S蛋白被插入4個帶正電荷的氨基酸, 能「靜電吸附」 黏上靶細胞受體帶負電的部份, 中和抗體無法擋住美其名為氣溶膠的「靜電吸附」, 免疫系統還未演化出對抗「靜電吸附」。
正電(鹼性胺基酸)的胺基酸,分別為組胺酸(Histidine His,H)、離胺酸(Lysine Lys, K)和精胺酸(Arginine Arg, R)
Receptor binding motif上面都標有位點, 多出來的 K528K529,R355K356R357,K535K537 ,K557K558

這「靜電吸附」造成任何疫苗都會 "突破性感染" , 且連非屬於ACE2受體的味覺細胞也會被感染,喪失味覺。
打過疫苗 ? 產生抗體 ? 只能擋掉 S蛋白嵌入人類ACE2受體
擋得住 靜電吸附 嗎 ? 擋不住 , 不是因為變種了才擋不住
雖然自 2020 年夏季以來,據報導出現了幾種 SARS-CoV-2 變種,它們可以逃避中和抗體。其中一些變種,例如 B.1.1.7 (alpha)、B.1.351 (beta)、B.1.1.248 (gamma) 和 B.1.617.2 (delta),這些變種比原始菌株更具傳染性,並且可以逃避中和抗體。
不過 , 忘記還有 細胞免疫 存在
病毒 SARS-CoV2 , 是以病毒外殼的Spike protein( S蛋白)嵌合人類ACE2受體 , 當疫苗進入人體內,會遇到先天免疫系統中的抗原呈現細胞antigen presenting cell (APC),像是巨噬細胞、樹突細胞。
這些細胞會吞噬掉疫苗顆粒,然後再分解這些疫苗顆粒,之後將部分抗原片段(S蛋白)表現在細胞表面,並轉移至淋巴結,進而活化適應性免疫系統的T淋巴細胞或B淋巴細胞,藉此產生具抗原特異性的細胞性免疫反應或體液免疫反應。
且會產生免疫記憶作用。當下次再有相同的Spike protein( S蛋白)的病原體侵入體內時,就能讓人體很快辨識,再次產生免疫反應,且會比之前來得快又強。
疫苗促進B淋巴細胞產生中和抗體 ,擋住 S蛋白嵌入人類ACE2受體 。
疫苗促進T淋巴細胞進行被感染細胞清除 , CD4+ T細胞活化殺手CD8+ T細胞後,細胞毒性T細胞(CTLs, killer T cells)負責殺傷被病毒感染的細胞。清除掉病毒
打疫苗雖然擋不住感染 , 病毒仍然會進入人體被驗到PCR陽性。但打疫苗後 T細胞會記憶住這個病毒 ,將來病毒進來後, 會活化殺手細胞展開毒殺。 最終清除掉病毒。疫苗能減少重症及死亡 。
2.天然免疫力 ??????
但是SARS-2抗體生成需要時間 , 這個病毒產生抗體IgG是 10 -21 天 , 達到足夠抗體力價要接近20天
但是這個SARS-2病毒的潛伏期 5.3 天, 症狀持續 5.8天
早在抗體生成之前 , 已經發病轉重症肺炎了
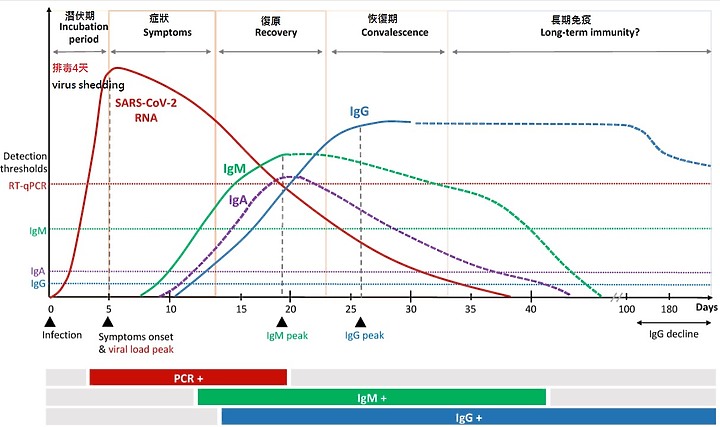
病毒跑得比抗體生成快 , 如何 天然免疫 ????
根本不是天然免疫 ?
是存在其它冠狀病毒的交叉免疫保護
血清陽性率研究表明,最常見的是 OC43,其次是 NL63、HKU1,最後是 229E。
許多未感染過新冠病毒, 也沒打過疫苗的人,體內卻早已存在對抗新冠病毒SARS-CoV-2的交叉反應抗體
美國曾經收集2019大流行前的血液樣本, 發現大流行前的血清, 已經存在對 SARS-CoV-2 的交叉反應抗體, 推測這是之前感染類似普通感冒OC43,NL63、HKU1等輕微症狀冠狀病毒親戚 ,如同牛痘對人痘(天花)有交叉反應 , 先前其它種類的冠狀病毒感染對 SARS-CoV-2這個親戚也產生了交叉免疫反應。
有交叉保護這能解釋是為何 有80%的人無症狀感染 ? 輕症? 無交叉保護會重症死亡?
老年人缺乏 交叉反應性 T 淋巴細胞 , 之前感染人類冠狀病毒 OC43 和 NL63, 難以對 SARS CoV-2有保護, 解釋了60 歲以上的老年人為何佔重症死亡率95% 以上。
3.天然抗體比疫苗強13倍 ??
沒有看過 這種報告
隨便找一篇 , BNT 和 Moderna 都高於 自然感染
Coronavirus disease 2019 vaccine response in pregnant and lactating women: a cohort study
AJOG | VOLUME 225, ISSUE 3, P303.E1-303.E17,
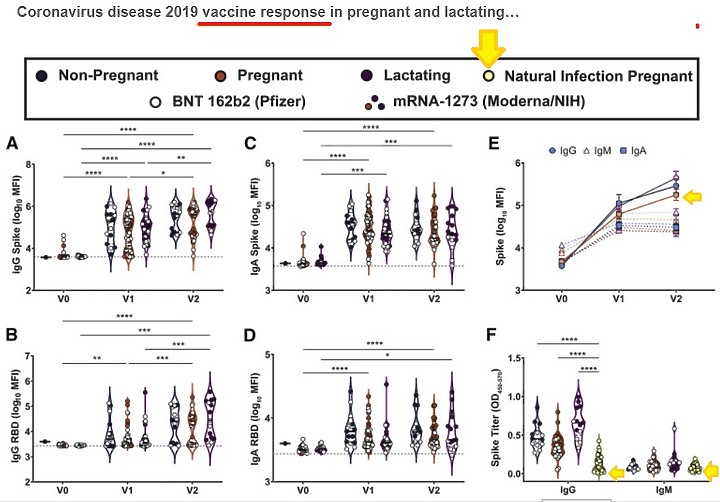
疫苗有效的指標 , 都會納入對比康復者的血清抗體 , 對比之後比較低的疫苗,根本是開發失敗, 不可能上市
是之前感染過SARS-2及其它種類的冠狀病毒 , 再打疫苗之後, 等同於booster, 抗體會更快反應及力價會更高
問題在於 ,大多數患者根本不知道自己曾經感染過 OC43 和 NL63 等等其它種類的冠狀病毒 , 當再感染SARS-2之後, 其實不是primary infection , 而是等同於 Booster , 抗體可能高於只打一劑疫苗者
4. 疫苗如何導致死亡傷殘?
是因為這個SARS-2病毒所選擇的受體是 ACE2
因為這個病毒的設計是選擇受體為 ACE2 (angiotensin-converting enzyme 2) 血管收縮素轉化酶 , 這是一種跨膜的結構域及細胞通道。
血管收縮素II具有高效的收縮血管作用,從而使血壓升高。
ACE2通過轉化"血管緊張素 II"和增加 Ang(1-7)血管擴張,來拮抗相關血管緊張素轉換酶(ACE)的活性。
當病毒上的棘蛋白結合ACE2受體後,就能由此通道進到細胞內大量增生,導致感染,同時還會抑制ACE2原本穩定血管收縮與抗發炎反應 ,ACE2表現量的下降與數種心血管疾病有相關性。
由於這個病毒受體為ACE2, ,當疫苗模擬了病毒的S蛋白去結合了ACE2 , 就會暫時抑制了ACE2舒張血管降血壓的功能 。而所有的疫苗 , 包括AZ ,BNT, Moderna 才會都發生了心血管的不良作用
這對於原本有心血管疾病相關病患相當不利 , 打疫苗反而會引發"心血管疾病"發作 。
打疫苗雖然擋不住感染 , 病毒仍然會進入人體被驗到PCR陽性。但打疫苗後 T細胞會記憶住這個病毒 ,將來病毒進來後, 會活化殺手細胞展開毒殺。 最終清除掉病毒。疫苗能減少重症及死亡 。
https://www.gov.uk/government/publications/covid-19-vaccine-surveillance-report
英國COVID-19 疫苗監測報告
有關 COVID-19 疫苗在現實世界中的有效性和影響的數據。
英國公共衛生部的看法和您相反 , 不是倒過來這樣說 , 它們公布的圖表是說
如果沒打疫苗 , 感染率和死亡率 盛行率 就是上面那條紅線 ,是打了疫苗才降低到下面那條 藍線
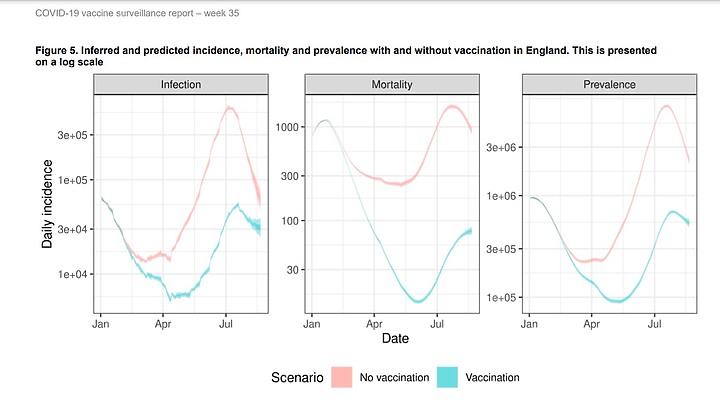
有打疫苗(藍線)和沒打疫苗(紅線) ? 在感染率infection(最左那欄)接近 , 原因就是 病毒能"靜電吸附" , 抗體擋不住感染
但是死亡率Mortality(中間那欄)和盛行率Prevalence(最右那欄)就能看出 , 紅線和藍線有一段距離 , T細胞被活化清除了病毒
疫苗多保護了多少人 ? 英國公共衛生部 說預防了14萬三千人住院 , 避免了醫療崩潰

選擇受體為 ACE2, 由於ACE2受體在NL63也有 , 這造成如同登革熱 , 二次接觸抗原, 可能發生抗體依賴增強作用,Antibody-dependent enhancement(ADE)
以及immune complexes免疫複合體 , 與補體結合後, 會引發自體免疫(第三型hypersensitivity)?
5) Covid無藥可醫其實是謊言
Available Compounds With Therapeutic Potential Against COVID-19: Antimicrobial Therapies, Supportive Care, and Probable Vaccines
對 COVID-19 具有治療潛力的可用化合物:抗菌療法、支持性護理和可能的疫苗
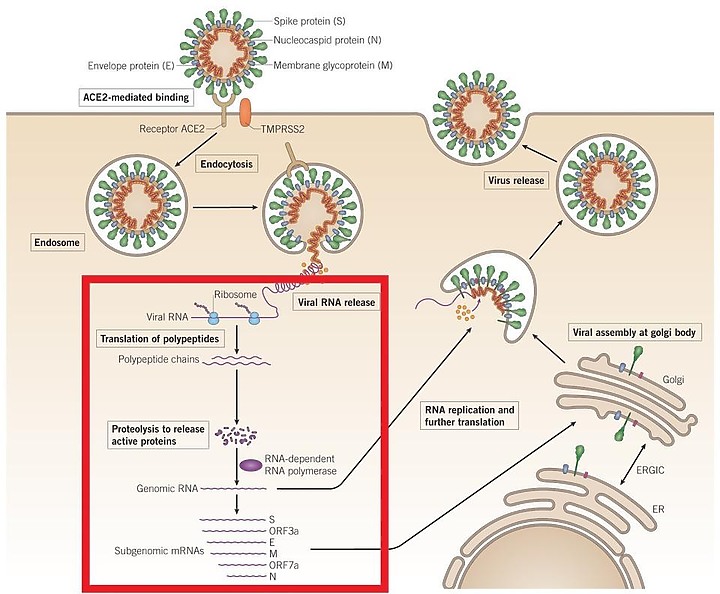
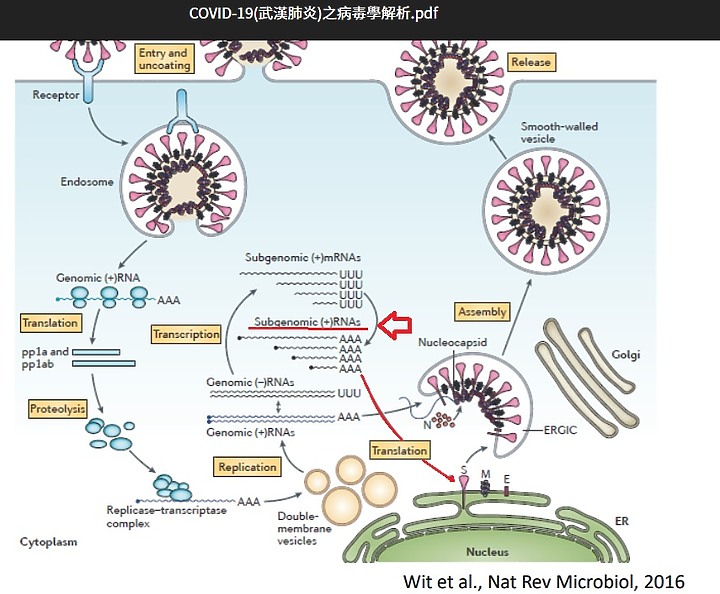
下圖: SARS-CoV-2 的生命週期及其可能的抑製劑。SARS-CoV-2的S 蛋白與由絲氨酸蛋白酶 TMPRSS2 引發的細胞的血管緊張素轉化酶 2 (ACE2) 結合。
病毒 RNA 在細胞質中出現以產生 PP1a 和 PP1ab 多蛋白,它們被切割形成非結構蛋白。
這些非結構蛋白通過複製和轉錄過程促進負股 RNA 的形成。這反過來又轉化為 N 蛋白。
另一組翻譯進入內質網-ERGIC-高爾基體以產生結構蛋白(S、M 和 E)。
最後,用 N 蛋白包裝病毒 RNA 並進一步組裝 S、M 和 E 蛋白,出芽形成 SARS-CoV-2 ,通過胞吐作用從受感染的細胞中釋放出來。
顯示在不同階段抑制 SARS-CoV-2 的各種藥物是 CQ/HCQ, Chloroquine氯喹//Hydroxychloroquine羥氯喹; ;L, Lopinavir洛匹那韋;R1,Ritonavir利托那韋;I, Ivermectin;伊維菌素;R,Remdesivir瑞德西韋,R2,Resveratro白藜蘆醇;D,Darunavir達蘆那韋;C,Camostat卡莫司他; ;F, Favipiravir法拉匹韋。
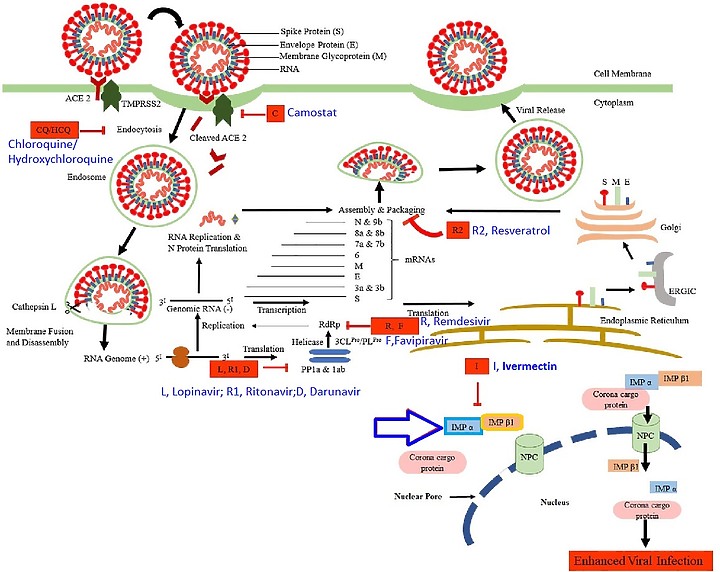
但是 藥物有半衰期 , 使用上都有限制 , 效果也是局限於某些"特定的條件下
其它藥物都在病毒複製的階段加以阻斷, 伊維菌素 Ivermectin涉及 IMPα/β1 的病毒核衣殼蛋白的信號依賴性核質關閉(Timani,2005;Wulan ,2015)。STAT1 轉錄因子的抗病毒活性被 SARS-CoV 輔助蛋白 ORF6 阻斷,導致 IMPα/β1 隔離在粗面內質網/高爾基體膜上
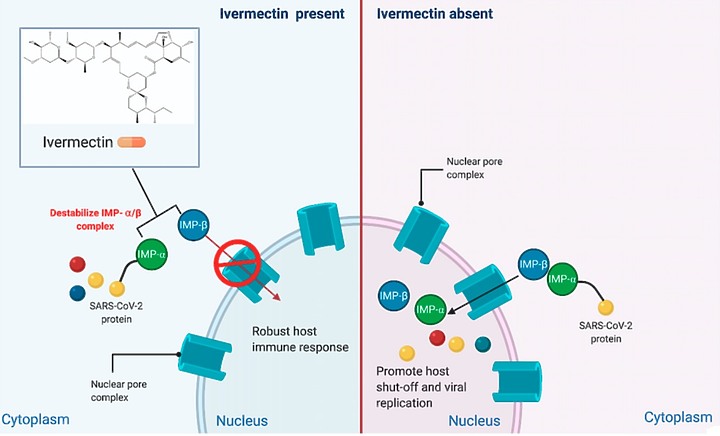
伊維菌素Ivermectin的抗 SARS-CoV-2 作用涉及伊維菌素Ivermectin先與 Impα/β1 異源二聚體的結合,導致其不穩定並阻止 Impα/β1 與病毒蛋白的結合。這樣可以防止SARS-CoV-2病毒的蛋白進入細胞核,導致有效的抗病毒反應
這是和病毒搶"位子" , 如果病毒已經搶先坐到那個受體的位置上 , 後到的伊維菌素Ivermectin 搶不到受體 ? 是無效的
藥物會代謝, 需要一直吃 .............
打疫苗 , 細胞免疫會記憶病毒
這個病 隔離檢疫 + 口罩消毒 + 疫苗 + 抗病毒藥 全都要 , 無法偏廢
6) 台灣人DNA優勢可以提早結束疫情
並沒有 , 亞洲人有重症基因 , 是非洲人 才有DNA優勢
日本沖繩科學技術大學教授帕博發現,武漢肺炎是否會演變為重症,與遺傳自尼安德塔人的重症基因相關。嚴重 COVID-19 風險相關的等位基因與 Vindija 33.19 尼安德特人基因組中的等位基因相似。這項研究發表在「自然」期刊(Nature)電子版
https://www.nature.com/articles/s41586-020-2818-3
The major genetic risk factor for severe COVID-19 is inherited from Neanderthals
Nature volume 587, pages610–612 (2020)
風險基因讓感染者染上武漢肺炎後 , 需要呼吸器供氧的可能性增加 3 倍。
現代人是出非洲之後 才碰上尼安德塔人 , 這個病還是和年齡, 三高等宿疾相關 , 非洲人很少受到重症基因影響。
南亞人約50%帶有重症基因 , 歐洲 約16%
只有非洲人沒有遺傳自尼安德塔人的重症基因 , 非洲除了南非 , 北非和歐洲人混血 , 其它地區都沒發生Covid-19 重症死亡的大流行
7) 哪些人打疫苗容易猝死?
因為受體是 ACE2 , 高齡 和三高 及 宿疾 都會是高危險群 , 患有心臟病和循環系統疾病以及糖尿病等現有健康問題的老年人更有可能。
英國、歐洲和美國的藥品監管機構表示,在 接種輝瑞和 Moderna 疫苗後,出現了少量心肌炎 (心肌炎症)和心包炎(心臟周圍的內膜炎症)病例。這些主要影響 12 至 29 歲的年輕男性,通常在第二次給藥後的兩週內。
AZ阿斯利康疫苗的 100,000 人中約有 1 人, 會發生特發性血小板減少性紫癜的輕度出血性疾病。血小板減少,這會導致更多的瘀傷、牙齦出血和內出血。大多數報告的病例發生在接種疫苗 2 週內的 60 歲以下女性 。
如果血栓發生在脈中腦(腦靜脈竇血栓形成,CVST)和腹部(內臟靜脈血栓形成)和動脈血液的血小板水平低,會併發出血。
對血栓和低血小板的組合的一個合理解釋是"免疫反應",導致與肝素治療患者(肝素誘導的血小板減少症,HIT)有時出現的情況相似的情況。
henrylai21 wrote:
看這篇: 台灣人基因有先天優勢不應懼怕病毒
而台灣呢?根據李博士的判斷,華人基因中有特殊的關鍵TCR與HLA,可以有效抵抗本次的病毒,他預估超過99.9%的台灣人都具備天然抵抗病毒的能力,因此這也解釋了台灣的疫情控制成績特別突出的原因之一,除了台灣人自覺,政府初期控制迅速之外,天然的基因其實也發揮了關鍵作用,讓新冠病毒在華人身上會突變產生Inactive mutant(失去感染活性的突變株),然後莫名奇妙消失(再次回顧敦睦艦隊染疫後全艦女友檢測皆為陰性的神奇案例),因此,台灣青壯年族群更不應該去排隊施打疫苗,特別是疫苗的突刺蛋白對於心血管系統的傷害,在國外的大量數據已經慢慢突顯出來。
(恕刪)
敦睦艦隊 磐石艦在海上1個月 , 病毒早就沒有感染力
這個病毒 隱藏潛伏很久嗎 ? 和匪諜一樣 ? 冠狀病毒不是1949 年 國防部中將參謀次長吳石 的角色?會藏起來 ?毒力永遠不會改變 ?
吳石和冠狀病毒是不同的
因為冠狀病毒是使用二套系統來複製
冠狀病毒 RNA 進入細胞質中,首先將 genomic RNA 轉譯出 RNA-dependent RNA 聚合酶及一些與病毒 RNA 合成有關的蛋白,形成之聚合酶便以 genomic RNA 為模版製造負股 RNA 。
負股 RNA 便可複製出genomic RNA 及轉錄出一組(約 5-7 個)具有相同 3’ 端 subgenomic mRNA(nested set of subgenomic mRNA)sgRNA,其在 5’ 端也都有相同的 leader sequence,用來製造病毒外殼蛋白。製造出病毒外殼的S蛋白才能嵌入人體細胞 。
此種分開兩套系統, 不連續轉錄方式(discontinuous transcription mechanism)是冠狀病毒的一大特性。
PCR是用來比對冠狀病毒主序列的RNA , 不是同時再驗由主序列分出來的那一小段sgRNA。 而製造感染所需的S蛋白是 sgRNA , 不是 主序列的RNA 。
PCR是用來比對冠狀病毒主序列的RNA , 驗出陽性是抓到了病毒核酸 , 無法知道這是年輕,在病毒的排毒期 Viral shedding 的5天內, 會抓交替感染的武漢病毒 ? 還是比對到 一株老化,存在8天以上 , 沒有sgRNA , 無法抓交替的老嫗病毒 。
PCR是比對出採到的檢體當中, 有武漢新冠病毒的核酸序列
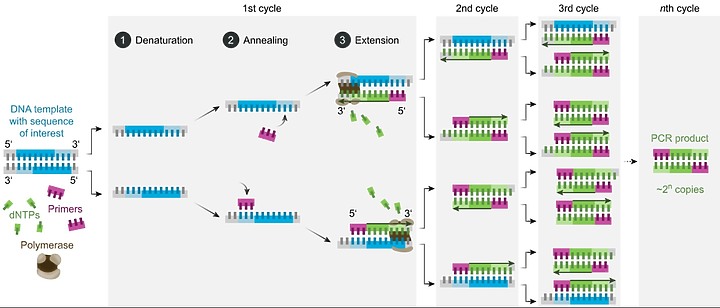
冠狀病毒是RNA病毒, 出先以反轉錄酶將冠狀病毒 RNA 轉變為互補 DNA, 藉由加熱讓 C-DNA 雙股分開,降溫讓「引子primer」找到目標基因接合,再升溫至 72℃讓引子延長複製 DNA,約 1-3 分鐘完成一個循環反應,可以增加 2 倍的核酸片段,經過多次(35~40 次)循環 CT值(Cycle Threshold)稱為「循環數閥值」後,可在大量擴增目的基因 。
在放大 2的多少次方之後 , 拼湊還原出的這段基因 可以和 SARS-2 冠狀病毒 比對出來, 這個『多少次方』就是檢體的CT值。
需要放大多少次方才還原出病毒核酸
原始的"檢體"中病毒核酸越多 ? 就越快, 越少『 2的多少次方』能還原出病毒
PCR 檢驗到 陽性? 根本不代表 "有感染能力" 或是 抓到 活病毒 ?只抓到核酸 !
CT 值 是能推估 能否感染 ?
SARS-2病毒有沒有"感染力" ?
主要依據是 這一篇文獻報告
Duration of infectiousness and correlation with RT-PCR cycle threshold values in cases of COVID-19, England, January to May 2020 separator

這篇報告除了測 檢體的 Ct值 , 也同時培養病毒 , 看病毒能不能在活的細胞內複製(造成CPE)
RT-PCR循環閾值(Ct)值與可否培養病毒密切相關。
用臨床檢體樣本接種Vero E6細胞,並在37°C,5%CO 2下孵育。每天檢查細胞的細胞病變CPE效應,直至14天
發現
所有藍色的點是能培養出病毒的, 全部都分佈於發病之前14天(發病前→發病時感染力最強)到發病後的13天之內
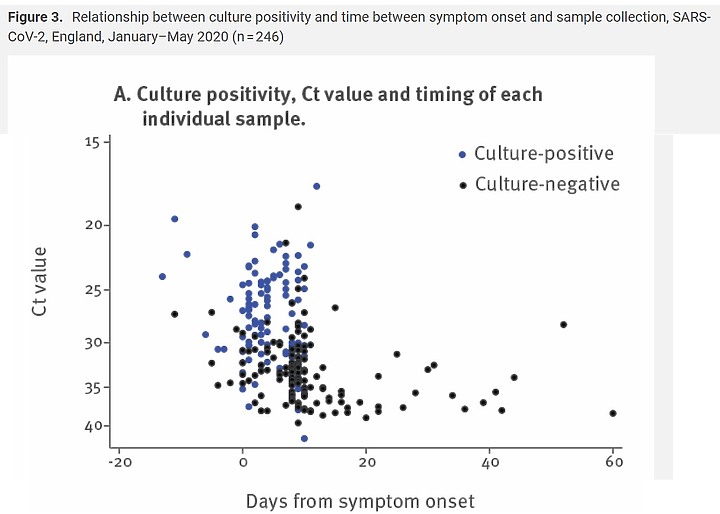
(1)Ct> 35的樣本中培養病毒的可能性降至8%
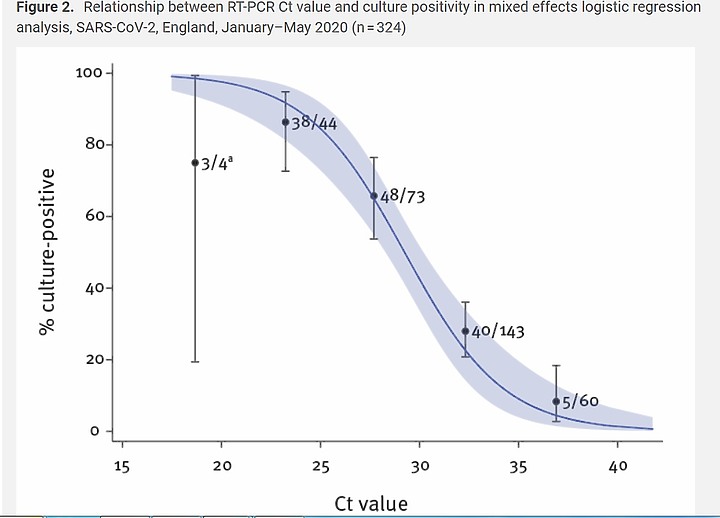
所以標準才訂為 Ct值35
(2)發病後10天降至6%
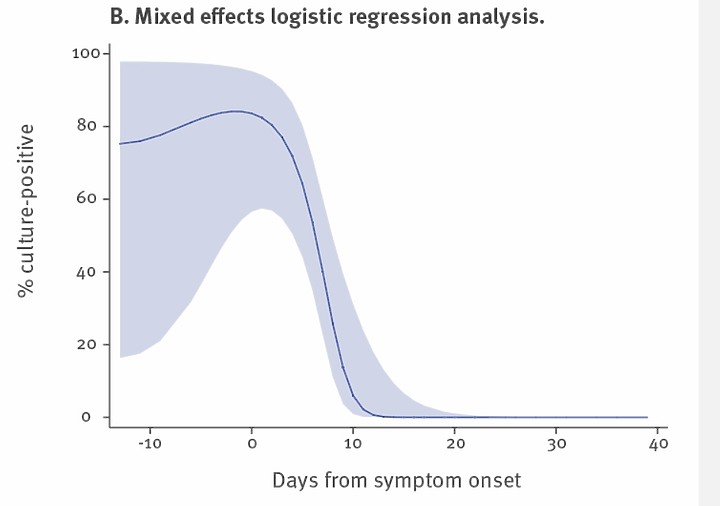
發病 13天之後的樣本 , 就再也養不出病毒了
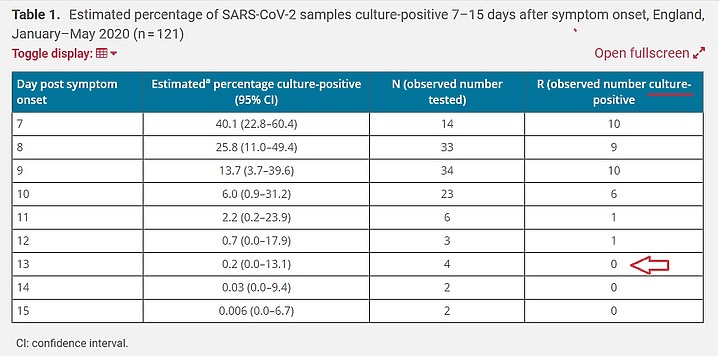
所以 檢疫期才訂為 14天
否則 就算是 60天之後 , 仍然能驗到 PCR為陽性
https://www.ecdc.europa.eu/en/covid-19/latest-evidence/transmission
歐盟衛生部綜合數篇報告的整理
Viral shedding 病毒排毒
Detection of viral RNA by PCR does not equate with infectivity, unless infectious virus particles have been confirmed through virus isolation and cultured from the particular samples.
由 PCR 測到 病毒的RNA , 並不代表有感染力 , 除非 透過 細胞培養分離並養 出病毒
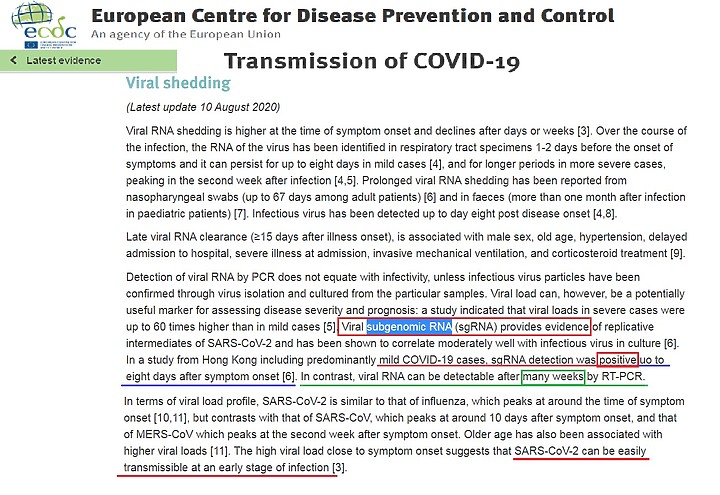
Viral subgenomic RNA (sgRNA) provides evidence of replicative intermediates of SARS-CoV-2 and has been shown to correlate moderately well with infectious virus in culture.
病毒次基因組 RNA (subgenomic RNA) 就是一項證據
病毒除了也會轉錄本身的 RNA , 也會轉錄出一系列較小片段的次基因體信使核糖核酸(subgenomic mRNA)。這些sgRNA也會利用細胞的蛋白質合成系統,做出病毒結構所需的棘(S蛋白)、膜、套膜和核鞘蛋白。
請看一下WHO 怎麼說
https://www.who.int/news-room/commentaries/detail/criteria-for-releasing-covid-19-patients-from-isolation
patients whose symptoms have resolved may still test positive for the COVID-19 virus (SARS-CoV-2) by RT-PCR for many weeks. Despite this positive test result, these patients are not likely to be infectious and therefore are unlikely to be able to transmit the virus to another person.
症狀已緩解的患者可能通過RT-PCR檢驗到COVID-19病毒(SARS-CoV-2)陽性達數週。儘管測試結果呈陽性,但這些患者不太可能具有傳染性,因此不太可能將病毒傳播給另一個人。
當前對傳播風險的了解
Current understanding of transmission risk
通過分子檢測(通常是RT-PCR)檢測到病毒RNA的存在,可以確認感染了導致COVID-19的病毒(SARS-CoV-2)。病毒RNA的檢測並不一定意味著一個人具有傳染性並且能夠將病毒傳播給另一個人。決定傳播風險的因素包括病毒是否仍具有復制能力,患者是否有症狀(例如咳嗽,可傳播感染性飛沫)以及與受感染個體相關的行為和環境因素。通常在感染SARS-CoV-2後5-10天,被感染的個體開始逐漸產生中和抗體。這些中和抗體與病毒的結合有望降低病毒傳播的風險。
Infection with the virus causing COVID-19 (SARS-CoV-2) is confirmed by the presence of viral RNA detected by molecular testing, usually RT-PCR. Detection of viral RNA does not necessarily mean that a person is infectious and able to transmit the virus to another person. Factors that determine transmission risk include whether a virus is still replication-competent, whether the patient has symptoms, such as a cough, which can spread infectious droplets, and the behavior and environmental factors associated with the infected individual. Usually 5-10 days after infection with SARS-CoV-2, the infected individual starts to gradually produce neutralizing antibodies. Binding of these neutralizing antibodies to the virus is expected to reduce the risk of virus transmission.

在患者症狀發生前後或疾病發作的前5天中,估計的傳播風險最高
, and the estimated risk of transmission was highest at or around the time of symptom onset and in the first 5 days of illness.
https://www.who.int/news-room/commentaries/detail/transmission-of-sars-cov-2-implications-for-infection-prevention-precautions
When do people infected with SARS-CoV-2 infect others?
感染SARS-CoV-2的人何時會感染他人?

病毒RNA的檢測並不一定意味著一個人具有傳染性並且能夠將病毒傳播給另一個人。
Detection of viral RNA does not necessarily mean that a person is infectious and able to transmit the virus to another person.
來自香港的一項研究(包括輕度COVID-19病例)在症狀發作到之後的8天, 都能檢測到sgRNA(能做出 Spike protein棘蛋白)為陽性 , Spike protein棘蛋白能嵌合到人類ACE2受體 。相反,可以在幾週之後 ,通過RT-PCR能檢測到病毒RNA ,但是卻驗不到 次基因體信使核糖核酸(subgenomic RNA)sgRNA 。
檢測到sgRNA(能做出外殼 Spike protein棘蛋白) , 表示能夠合成出能嵌合人類細胞的Spike protein棘蛋白 。
但是 PCR 是驗到有全序列的病毒核酸存在 , 這個全序列的核酸 無關 感染 與否
PCR 60天後仍能還原出全序列的病毒核酸 , 但是會製造嵌入人體S蛋白的sgRNA(由主序列分出), 早就不存在了
「凱撒的歸凱撒,上帝的歸上帝」
內文搜尋
X