高端疫苗採購合約近日爭議再起,疫苗的保護力也引發外界關注。事實上,WHO(世界衛生組織)資料庫收錄一篇〈高端新冠肺炎疫苗真實世界保護效益〉論文,結論指採用次單位蛋白質的高端疫苗,保護力遠優於AZ,和莫德納及輝瑞BNT相當,重症保護力也優於AZ、輝瑞BNT與莫德納。
該論文是2021年3月到2022年9月的研究,透過疾管署的國家免疫資訊系統及通報系統回報資料統計,研究結果指出,「與3劑疫苗接種相比,接種3劑AZ疫苗,或將其作為基礎劑再搭配mRNA或蛋白質為基礎的疫苗,其嚴重風險較高(發病率為 0.390-0.762)。其次是默德納mRNA(發病率為 0.316-0.471)、高端MVC(發病率為 0.044-0.196)和輝瑞BNT(發病率為 0.061-0.197)。
有關死亡結果,AZ的致命風險較高(發病率為 0.127-0.269),其次是默德納mRNA(發病率為 0.086-0.125)、高端MVC(發病率為 0.013-0.064)和輝瑞BNT(發病率為 0.015-0.045)。
在疫情肆虐當下,國人多數先施打了AZ疫苗,之後才採用混打方式接種追加劑,該項論文指出,「以AZ或其作為基礎劑的疫苗保護效益,對嚴重病例的疫苗保護效益為65.9%至77.7%;mRNA疫苗保護效益為86.4%至96.1%;蛋白質為基礎劑的疫苗(高端)保護效益為91.4%至96.2%。對死亡的疫苗保護效益呈現相似的模式,保護效益為60.9%至73.7%,88.2%至96.2%,以及90.3%至95.6%。」
換句話說,在真實世界的保護效益,高端是優於AZ,與默德納、輝瑞BNT相當,而在重症保護力上,也有相同效果。
完整論文: https://pesquisa.bvsalud.org/global-literature-on-novel-coronavirus-2019-ncov/resource/pt/covidwho-2316428
https://www.msn.com/zh-tw/news/living/%E9%AB%98%E7%AB%AF%E7%96%AB%E8%8B%97%E4%BF%9D%E8%AD%B7%E5%8A%9B%E6%88%90%E7%88%AD%E9%BB%9E-who%E8%B3%87%E6%96%99%E5%BA%AB%E8%AB%96%E6%96%87-%E5%84%AA%E6%96%BCaz%E9%87%8D%E7%97%87%E4%BF%9D%E8%AD%B7%E5%8A%9B%E6%9B%B4%E5%8B%9D%E8%8E%AB%E5%BE%B7%E7%B4%8Dbnt/ar-AA1mJIgb?ocid=msedgdhp&pc=EDGEDB&cvid=35c37b66beda4894a5dd9ea20e04abd9&ei=38
engcalvin wrote:
中國的疫苗,一做出來就開始施打
美國的默德納疫苗,也是沒有經過完整驗證就開始施打
不打確定會有大批的人死亡,看看中國武漢一開始的慘況,剛出來的病毒致死率非常高
各國政府都是「特准」疫苗施打
藥廠無法保證,所以是各國政府提出免責保證,藥廠才願意供應「未經完整驗證」的疫苗
我總覺得有一個暗黑勢力在刻意攻擊高端
攻擊高端應該是基於三個原因:
1.破壞台灣生技產業
2.打擊台灣政府
3.分化台灣
沒有任何國家對於自己的高科技產業,不出手協助,就算以兩倍價購買自己國內生產的疫苗也不為過
中國疫苗有效率這麼差,差到要「堅持清零」,中共、習皇都一路相挺,到病毒致死率降低為止
次情此景,打擊台灣生技產業,看來是很成功
陳時中 當時就宣布,人民可以自己選疫苗,並沒有規定
對照中國人只能打國產無效疫苗,應驗「三人成虎」、「人言可畏」
https://pansci.asia/archives/322952
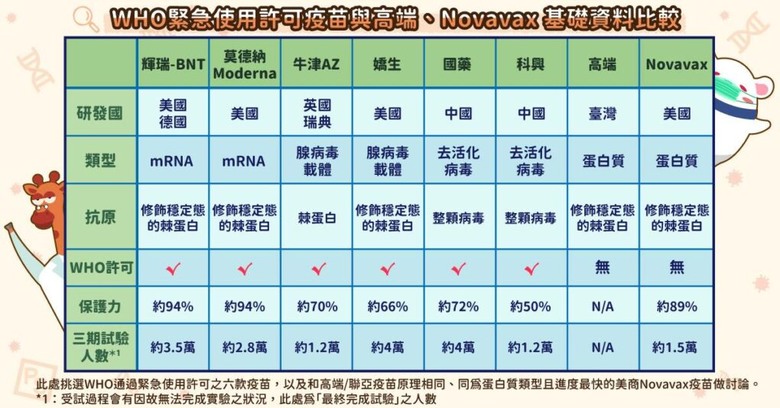
全面解析!8 種疫苗的基礎資訊
一、輝瑞-BNT 疫苗
由德國 Biotech 和美國輝瑞(Pfizer)合作推出。屬 mRNA 技術,內容為可轉譯(translation)出經修飾後穩定態的棘蛋白(spike protein, S-2P)的 mRNA。
-----廣告,請繼續往下閱讀-----
保存運輸嚴苛,須在 -80℃ 環境下運送。需施打兩劑,間隔 21 天。已公開、上網三期試驗數據。獲得世界衛生組織(WHO, World Health Organization)、美、英多國的緊急使用。
瑞輝-BNT 疫苗。圖/U.S. Secretary of Defense
以美國而言,專家委員會於 2020/12/10 全程直播討論該疫苗的科學證據(三期試驗書面數據於2天前向公眾公開)並支持提供美國民眾使用、2020/12/11 通過 16 歲以上民眾緊急使用許可、2021/05/10 放寬許可,12 歲以上皆可接種。
就以色列全國超大型的施打結果而言(近 120 萬人之數據),整體保護力約 94%,對 70 歲以上的年長者的保護力更高達 98%。而且當時以色列境內流行英國變異株(B.1.1.7),更顯示了輝瑞-BNT 疫苗抵禦英國變異株的能力。
而較令人擔憂之處,是全身性過敏反應的比例似乎較高,約 4.7 例/每百萬劑(資料更新至 2021/01/18,現行流感疫苗約 1.3 例/每百萬劑)。美國 CDC 建議,已知對聚乙二醇(PEG / Polyethylene glycol)等疫苗成份過敏之接種者,接種前和醫護團隊詳細討論;必要時可改選其他類型疫苗。
-----廣告,請繼續往下閱讀-----
二、莫德納疫苗
由美國莫德納(Moderna)推出。屬 mRNA 技術,內容為可轉譯(translation)出經修飾後穩定態的棘蛋白(spike protein, S-2P)的 mRNA。
保存運輸嚴苛,須在 -20℃ 環境。需施打兩劑,間隔28天。已公開、上網三期試驗數據。獲得WHO、美、英多國的緊急使用。
莫德納疫苗。圖/U.S. Air Force photo by Airman 1st Class Anna Nolte
以美國而言,專家委員會於 2020/12/17 全程直播討論該疫苗的科學證據 (三期試驗書面數據於 2 天前向公眾公開)並支持提供美國民眾使用、2020/12/18 通過 18 歲以上民眾緊急使用許可。
-----廣告,請繼續往下閱讀-----
就莫德納三期臨床數據而言(近 3 萬人之數據),整體保護力約 94%,對 65 歲以上的年長者的保護力約 86%。而針對英國變異株(B.1.1.7)的效力,實驗室數據顯示,莫德納疫苗誘發的抗體效力,未因變異株而減退。
而較令人擔憂之處,是全身性過敏反應的比例似乎較高,約 2.5 例/每百萬劑(資料更新至 2021/01/18 現行流感疫苗約 1.3 例/每百萬劑)。美國 CDC 建議,已知對聚乙二醇(PEG/Polyethylene glycol)等疫苗成份過敏之接種者,接種前和醫護團隊詳細討論;必要時可改選其他類型疫苗。
三、嬌生疫苗
由美國嬌生(Janssen Biotech)推出。屬腺病毒載體技術(Ad26),內容為可轉錄(transcription)、轉譯(translation)出經修飾後穩定態的棘蛋白(spike protein, S-2P)的活化、無複製能力的腺病毒。
-----廣告,請繼續往下閱讀-----
保存運輸友善、4℃ 環境。只要打一劑。已公開、上網三期試驗數據。獲得WHO、美、英多國的緊急使用。
嬌生疫苗。圖/New York National Guard
以美國而言,專家委員會於 2021/02/26 全程直播討論該疫苗的科學證據 (三期試驗書面數據於2天前向公眾公開)並支持提供美國民眾使用、2021/02/27 通過 18 歲以上民眾緊急使用許可。
就嬌生提交給美國政府的三期臨床數據而言(近 4 萬人之數據),整體保護力約 66%,對 60 歲以上的年長者的保護力約 76%(防止中重症)。
但在歐洲出現牛津接種後,發生多例罕見血栓併血小板低下症候群(TTS, Thrombosis with Thrombocytopenia Syndrome),且美國本土亦出現 6 例的類似情況。美國於 2021/04/13 暫停嬌生疫苗使用,審查後認為利益大於風險,於 2021/04/23 重新恢復使用。
-----廣告,請繼續往下閱讀-----
四、牛津疫苗(AZ 疫苗)
由英國阿斯特捷利康(AstraZeneca)和牛津大學合作推出。屬腺病毒載體技術(ChAdOx1),內容為可轉錄(transcription)、轉譯(translation)出經修飾後穩定態的棘蛋白(spike protein, S-2P)的活化、無複製能力的腺病毒。
保存運輸友善、4℃ 環境。需施打兩劑,間隔 8~12 週。已公開、上網三期試驗數據。獲得WHO、英、日多國的緊急使用。
AZ 疫苗。圖/Arne Müseler.
牛津疫苗的三期臨床試驗數據,於 2020/12/08 發表於《柳葉刀 / The Lancet》。以英國而言,於 2020/12/30 通過 18 歲以上民眾緊急使用許可(未公開會議內容)。
-----廣告,請繼續往下閱讀-----
就牛津疫苗的三期臨床試驗數據而言(超過 1 萬人之數據),整體保護力約 70%。在最初的三期試驗中,因數據不足,故無法了解對年長者的保護力。但在今年(2021年)四月的研究中發現,單劑牛津疫苗對 70 歲以上年長者的保護力約 80 %。
2021 年三月上旬,歐洲各國出現了數十件血栓的病例、數人死亡。當時,歐洲多國預防性地暫停民眾接種牛津 AZ 疫苗。
經過調查,歐洲藥品管理局(EMA, European Medicines Agency)和英國藥品和醫療產品監管署(MHRA, Medicines and Healthcare products Regulatory Agency)於 2021/04/07 發佈聲明,認為牛津疫苗可能會罕見地引發血栓併血小板低下症候群(TTS, Thrombosis with Thrombocytopenia Syndrome),但由於疫情嚴峻,接種疫苗的利益仍大於風險,持續推動民眾施打。
牛津疫苗有進行疫苗混打的實驗,混打的疫苗有輝瑞-BNT、Novavax 等。就今年(2021年)五月、用牛津和輝瑞-BNT混打的研究發現,受試者的不適感會變強、比例變多(相較於只打牛津,或只打輝瑞-BNT)。
-----廣告,請繼續往下閱讀-----
五、高端疫苗
高端疫苗(MVC-COV1901)由台灣生技公司高端疫苗(Medigen Vaccine Biologics.)推出,屬蛋白質技術,內容為修飾後穩定態的棘蛋白(spike protein, S-2P)和佐劑(鋁鹽、CpG)。
保存運輸友善、4℃ 環境。需施打兩劑,間隔 28 天。尚未進行三期試驗。尚未獲得任何國家許可。
目前處在二期臨床試驗階段,受試者已在 2021/04/28 接種完第二劑,已於 06/10 解盲。就一期臨床試驗數據顯示,施打疫苗後產生之抗體強度,接近、或高於感染 COVID-19 後康復者體內的抗體強度。
高端疫苗第二期試驗已完成第二劑施打。圖/高端疫苗
六、Novavax 疫苗
由美國 Novavax 推出。屬蛋白質技術,內容為修飾後穩定態的棘蛋白(spike protein, S-2P)和佐劑(皂苷)。
保存運輸友善、4℃ 環境。需施打兩劑,間隔 21 天。已公開、上網三期試驗數據。尚未獲得任何國家許可。
Novavax 三期臨床試驗結果,於 2021/05/14 發表於預印本medRxiv。超過 1 萬 5 千人之數據顯示,整體保護力約 89%,針對英國變異株(B.1.1.7)的保護力約 86%,對 65 歲以上年長者保護力約 88%。
Novavax 三期臨床試驗結果。圖/medRxiv
七、科興疫苗
由中國科興控股生物技術推出,國內通常稱「科興疫苗(CoronaVac)」。屬不活化病毒技術,內容為整顆新型冠狀病毒(SARS-CoV-2)和佐劑(鋁鹽)。
保存運輸友善、4℃ 環境。需施打兩劑,間隔 14 天。已公開、上網三期試驗數據。獲得世界衛生組織(WHO)、中國、菲律賓等多國的緊急使用。
科興疫苗。圖/Elenktra
科興三期臨床試驗結果,於 2021/04/14 發表於預印本。超過 1 萬 2 千人之數據顯示,整體保護力約 50%。但數據有以下令人擔憂之處:
年長受試者過少:
科興疫苗試驗裡的受試者,60 歲以上僅佔 5%。相較於其他疫苗,明顯過少(相較於最少的莫德納、Novavax,65 歲以上受試者均達 25%)。因此科興疫苗對年長者的保護力數據,因樣本數少而有待論定。
體內抗體似乎無法長期維持:
觀察接種後累積感染曲線,科興疫苗的接種者中,新感染者仍然持續上升,且沒有出現平緩的傾向。此點和其他疫苗表現有很大的差距,可能是抗體衰減迅速,導致接種者失去保護力;或當地病毒變異快速,已超脫科興疫苗原始設計。
八、國藥疫苗
由中國國藥集團推出,國內通常稱「國藥疫苗(BIBP)」。屬不活化病毒技術,內容為整顆新型冠狀病毒(SARS-CoV-2)和佐劑(鋁鹽)。
保存運輸友善、4℃ 環境。需施打兩劑,間隔 21 天。已公開、上網三期試驗數據。獲得 WHO、中、印尼多國的緊急使用。
國藥三期臨床試驗結果,於 2021/05/26 發表於《美國醫學會雜誌 JAMA》。近 4 萬人之數據顯示,整體保護力約 72%(國藥疫苗使用兩病毒株為原料,本文取保護力較低之數據)。但數據有令人注意之處:包含安慰劑組,60 歲以上年長者無人染疫,因此無法評估該疫苗對年長者的保護力。
國藥三期試驗結果。圖/JAMA
編按:於 2021/6/7 晚間補充以下文字。
但國藥疫苗的三期實驗設計,有以下令人擔憂之處:
1) 相較於其他疫苗三期受試者的年齡 (輝瑞-BNT:52歲、嬌生:52歲、Novavax:56歲),國藥受試者相當年輕,平均僅有36.1歲。通常而言,疫苗在年長者體內產生抗體的效果較弱,且COVID-19又對年長者的危害甚劇。因此疫苗三期試驗應盡量招募足夠多的年長者,才能更好體現試驗的價值。
2) 相較於其他疫苗三期受試者的女性佔比 (輝瑞-BNT:49.4%、嬌生:45%、莫德納:47.3),國藥女性受試者非常少,僅佔15.6%。通常而言,疫苗在女性會產生更多、更難受的不良反應,況且科學界不清楚性別對於新疫苗的影響,因此疫苗三期試驗應讓受試者性別比例相近,才能更好體現試驗的價值。
engcalvin wrote:
高端疫苗保護力成爭點...(恕刪)
https://udn.com/news/story/123866/7693352
鄭正鈐揭露高端錄音 批高層利用美國衛生院名聲背書
2024-01-08 13:26 聯合報/ 記者
張睿廷
/台北即時報導
國民黨立委鄭正鈐(右)今天開記者會,指出高端董事會第四段錄音檔內容,質疑高端利用美國國家衛生院的名聲,牟取政府補助、炒高股價,誤導投資大眾。痛批民進黨政府護航高端,成為高端股票異常起伏的幫兇,坑殺無辜股民。圖/鄭正鈐提供
國民黨立委鄭正鈐(右)今天開記者會,指出高端董事會第四段錄音檔內容,質疑高端利用美國國家衛生院的名聲,牟取政府補助、炒高股價,誤導投資大眾。痛批民進黨政府護航高端,成為高端股票異常起伏的幫兇,坑殺無辜股民。圖/鄭正鈐提供
國民黨立委鄭正鈐今天舉行記者會,公布高端董事會第四段錄音檔內容,質疑高端利用美國國家衛生院名聲,牟取政府補助,炒高股價,誤導投資大眾,民進黨政府護航高端,成為高端股票異常起伏的幫兇,坑殺無辜股民。
鄭正鈐指出,高端疫苗副董事長陳燦堅2020年4月27日表示,高端疫苗上市有望,與美國國家衛生院同步,這個消息讓高端的股價從4月27日的54.5元,漲到7月15日的134.5元,這一波的漲勢高達246%。
他表示,高端2020年4月對外說疫苗上市跟美國國衛院同步,結果到了8月7日董事會的錄音檔顯示,高端寫好一篇疫苗成效的學術論文,希望美國國衛院掛名發表出去,美國國衛院覺得高端貢獻不夠,不願掛名背書。高端卻還跟對方說,只要掛名就是貢獻啦。
鄭正鈐說,高端不斷對外宣稱與美國國衛院合作無間,美國國衛院根本不願意在高端論文掛名,高端難道不是利用美國國衛院的名聲,欺騙國人,騙衛福部的補助。
鄭正鈐表示,高端股價從2020年4月27日的54.5元,一路攀升至2021年5月17日的417元,漲勢高達765%。高端內線炒股傳聞不斷,金管會更是移送九次異常交易分析報告。高端股價漲跌異常,爆出股東名冊內有上千名民進黨員,有多位民進黨重要人士,高端與民進黨政府之間,是否涉入內線交易與官商勾結,留下太多可議之處,檢調應深入調查。
鄭正鈐指出,高端連二期的人體試驗都沒完成,民進黨政府就急著讓高端通過緊急使用授權(EUA),還為高端打造獨步全球的免疫橋接,替代三期臨床試驗。食藥署通過高端疫苗EUA,審查過程不公開透明,事前刻意更換反對免疫橋接的審查委員。
鄭正鈐說,民進黨總統候選人賴清德贊成公開高端疫苗採購合約的行為,是騙選票。民進黨是執政黨,國會過半數,如果真有心要公開合約,馬上就可以公開,賴清德喊公開喊了10天,到現在都沒公開,這就是典型的隨便講講,騙選票。
內文搜尋
X